Introduction
황색포도상구균(Staphylococcus aureus)은 분비하는 장독소를 통하여 식중독을 일으키는 대표적인 식중독 원인균 중 하나이다(Bae and Park, 2007). 황색포도상구균으로 인한 식중독을 일으키는 원인 식품으로는 일반적으로 곡류 및 가공품, 복합조리 식품, 유제품 등이 있으며, 황색포도상구균 독소가 함유된 이들 식품을 섭취할 경우 짧은 시간 내(평균 3시간)에 구토, 설사, 복통과 같은 증상을 일으킨다(KCDC, 2018).
최근 10년간 우리나라에서 황색포도상구균에 의한 식중독 사고는 매년 평균 16.7건, 환자수 6백여명으로 지속적으로 발생하고 있으며, 주로 단체급식을 제공하는 곳에서 발생하여 그 피해가 매우 크다고 할 수 있다(MFDS, 2016).
황색포도상구균 독소는 20가지 이상이며 이 중 staphylococcal enterotoxin A (SEA)와 staphylococcal enterotoxin B (SEB)가 식중독을 가장 많이 일으키는 것으로 알려져 있다(Irina et al., 2010). 황색포도상구균 독소는 끓여도 파괴되지 않을 정도로 열에 매우 강하며, 건조, 냉장, 냉동, 상온 등 대부분의 유통조건에서 안정된 상태로 존재하여 식중독 위험을 내재하기 때문에 각별한 주의가 요구된다(Cho et al., 2011). 식중독을 일으키기 위한 장독소 최소인체위해용량은 약 100 ng이며, 이러한 정도의 장독소를 생성하기 위해서는 황색포도상구균의 농도가 105 CFU/g 정도여야 한다(MFDS, 2015).
기존의 황색포도상구균 독소 시험법은 확인시험 등 과정이 복잡하고 장시간이 소요되며 대략적인 균의 농도로 독소량을 추정해 내는 방법이기 때문에 식중독 발생 시 신속한 원인규명 및 조치를 취할 수 없는 단점을 지니고 있다. 황색포도상구균 독소를 간편하게 검출하기 위하여 효소면역측정법(enzyme linked immunosorbent assay, ELISA), 한천확산정량법(gel-diffusion method), 역수신라텍스응집법(reversed passive latex agglutination, RPLA) 등의 방법들이 개발되었으나, 이들 방법 역시 과정이 복잡하고 숙련된 전문가가 필요하여 누구나 쉽고 빠르게 황색포도상구균 독소를 검출할 수 있는 신속 검사기술의 개발 필요성이 제기되고 있다.
최근 여러 분야에서 활용되고 있는 측방유동형 간이 진단키트는 저렴한 가격, 신속검사, 높은 감도, 사용의 편이성, 쉽고 편한 보관 등의 장점 때문에 현장에서 식품안전성을 검사하는 도구로서의 활용 가능성이 아주 높다. 간이 진단키트는 항원과 항체의 특이적인 면역반응을 기반으로 하며, 나노 금입자, 탄소입자, 실리카 입자, 폴리머, 양자점 등 색을 띄는 입자를 사용하여 검사 대상의 유무를 확인한다(Posthuma-Trumpie et al., 2009). 이러한 간이 진단키트는 살모넬라 식중독균(Kim et al., 2011), 곰팡이 독소(Anfossi et al., 2011), 탄저균 포자(Wang et al., 2013)를 검사하기 위해 개발된 바 있다.
측방유동형 간이 진단키트의 검출 성능과 관련된 주요 요인으로는 항체, 표지용 색입자, 니트로셀룰로오스 막 등이 있으며, 진단키트의 검출 성능을 높이기 위하여 항체 대용의 압타머, 일반적인 표지물질로 사용되는 금입자를 대체할 수 있는 탄소입자, 형광입자, 자석입자 등에 대한 연구가 수행되고 있다 (Kim et al., 2015).
본 연구는 식중독 사고의 주요 원인물질 중 하나인 황색포도상구균 독소 B를 신속하게 검출할 수 있는 측방유동형 간이 진단키트를 개발하고자 수행되었다. 간이 진단키트의 표준물질로 가장 많이 사용되는 금입자 대신 새로운 표지물질인 셀룰로오스 나노입자를 이용하여 검출 성능을 향상하고자 하였으며, 개발된 간이 진단키트의 황색포도상구균 독소 B (SEB) 검출 성능은 인산완충 용액 및 식품시료를 이용하여 조사하였다.
Materials and Methods
간이 진단키트의 제작 및 검출 원리
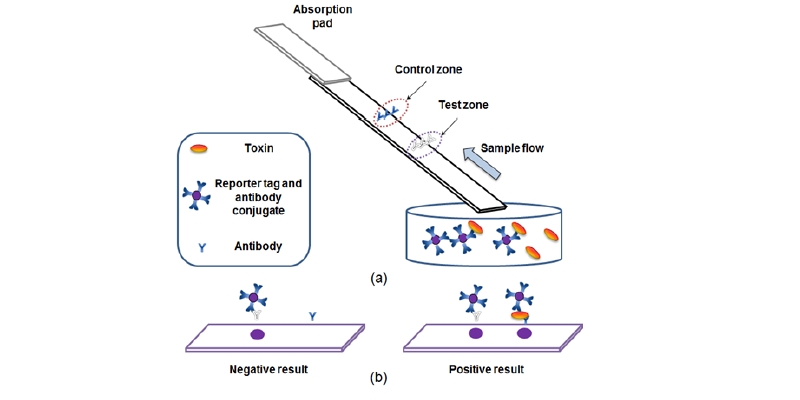
간이 진단키트는 완전한 형태의 진단키트 제작에 따른 시간과 비용을 절약하기 위하여 Fig. 1(a)와 같이 결합패드를 사용하지 않고 니트로셀룰로오스막과 흡수패드로 구성하였다. 검출 시험은 표지물질-항체 결합물 5 µL, 그리고 검출대상인 SEB와 전처리 물질을 포함하는 버퍼 110 µL를 96구 플레이트에서 30분간 먼저 반응시킨 다음, 진단키트의 한 끝을 담그는 방법으로 수행하였다. 시료 내 SEB 유무에 따라 표지물질-항체 또는 표지물질-항체-독소 결합물이 생성되고, 이 결합물은 시료 용액과 함께 모세관 현상에 의해 니트로셀룰로오스막을 따라 흡수패드 쪽으로 이동한다. 이동하는 결합물은 니트로셀룰로오스막에 SEB 검출 항체를 도포한 검사점이나 토끼 단백질 검출 항체를 도포한 컨트롤점에 포획되어 색을 띄는 점을 형성하게 된다.
니트로셀룰로오스막의 검사점은 표지물질에 결합시킨 항체와는 다른 종류의 SEB 항체를, 그리고 컨트롤점은 표지물질에 결합된 항체에 반응하는 anti-rabbit 항체를 각각 도포한 다음 37℃ 에서 1시간 건조하여 형성시켰다. SEB의 포획을 위한 검사점은 니트로셀룰로오스막의 가장자리에서 10 mm 떨어진 부위의 중심선 근처에 마이크로피펫을 이용해 1 μL의 SEB 항체를 떨어뜨리는 방식으로 제작하였다. SEB 항체는 인산완충 용액에 용해된 1 mg/mL 농도의 것을 사용하였다. 컨트롤점은 인산완충 용액에 1 mg/mL 농도로 용해시킨 anti-rabbit 항체 용액을 검사점에서 흡수패드 쪽으로 15 mm 떨어진 위치에 도포하여 제작하였다.
간이 진단키트를 이용한 SEB 검사 결과는 Fig. 1(b)와 같이 해석된다. 검사점과 컨트롤점 모두 짙은 색의 점이 형성되면 시료에 검출한계 이상의 SEB가 포함된 것으로 진단되며, 컨트롤점만 짙은 색이 형성되면 시료에 포함된 SEB의 농도가 낮거나 없는 것으로 진단된다. 검사점과 컨트롤점 어느 곳에서도 배경과 구분되는 색 변화를 나타내지 않으면 항원 · 항체 결합 실패 등의 이유로 실험이 잘못된 것으로 진단된다.
진단키트 재료 및 시약
SEB의 검출유무를 색으로 나타내기 위한 사용되는 표지물질은 Bioassay work사(MD, USA)의 40 nm 금 나노입자 또는 DCN 사(CA, USA)의 셀룰로오스 나노입자를 이용하였으며, 색입자와 결합하는 SEB 표지 항체 및 표준 SEB는 Toxin technology사(FL, USA)의 것을 이용하였다. 또한 검출부에 사용되는 SEB 포획용 항체는 Sigma사(MO, USA)에서, 컨트롤점에서 SEB 표지 항체를 포획하는 anti-rabbit 항체는 KPL사(MA, USA)에서 구입하였다. 니트로셀룰로오스 막과 흡수패드는 Millipore사(MA, USA), 간이 진단키트 전처리를 위해 사용한 Tween-20은 MBcell사(Seoul, Korea), 자당(sucrose)과 인산완충 용액(phosphate buffered saline, PBS)를 비롯한 기타 시약은 Sigma사의 제품을 사용하였다.
황색포도상구균 독소 검출 실험 방법
간이 진단키트를 이용한 SEB 검출 실험은 정제된 표준 SEB를 인산완충 용액에 103 - 10-1 ng/g으로 희석시킨 시료를 이용하여 수행하였다. 실제 농식품 시료에 대한 간이 진단키트의 적용 가능성은 닭고기 세척 버퍼에 103 - 10-1 ng/g의 농도로 접종한 SEB를 이용하여 수행하였다. 닭고기 세척 버퍼는 시중에서 구입한 닭 가슴살 부위 25 g을 225 mL의 인산완충 용액에 넣고 교반하는 방법으로 제조하였다. 또한, 황색포도상구균 독소 B 검출용 간이 진단키트의 다른 독소에 대한 선택성은 유사한 황색포도상구균 독소인 SEA와 SEC를 이용하여 조사하였다.
간이 진단키트를 이용한 SEB 검출 실험 결과는 탁상형 스캐너(CanoScan Lide 120, Canon, USA)를 이용하여 진단키트의 영상을 획득한 다음, 색변화가 발생한 검사점의 밝기를 영상처리 프로그램(ImageJ 1.51, NIH, USA)을 이용하여 측정하였다. SEB 검출로 인한 검사점의 색변화는 검사점의 밝기 평균값을 계산하고 이 값에서 주위 배경의 밝기 평균값을 빼는 방법으로 구하였다. 진단키트의 SEB 검출한계는 SEB가 들어 있지 않은 PBS 또는 닭고기 버퍼만의 시료 검사 결과 평균값에 3배의 표준편차를 더한 값 이상의 밝기 변화를 나타내는 SEB 농도로 정하였다.
Results and Discussion
금입자를 표지물질로 하는 진단키트를 이용한 SEB 검출
금입자를 표지물질로 사용하여 제작된 간이 진단키트의 SEB 검출 성능은 농도가 다른 SEB (103 - 10-1 ng/g)가 포함된 인산완충 용액 시료를 이용하여 조사하였다. 간이 진단키트를 시료와 금입자-항체 결합물이 섞여있는 용기에 담그면 이 시료용액은 모세관현상에 의해 흡수패드 쪽으로 흐르게 된다. 시료에 포함되어 있는 SEB는 SEB 항체-금입자 결합물과 항원-항체 반응을 일으켜 SEB-SEB 항체-금입자의 결합물을 형성한다. 이 결합물은 니트로셀룰로오스 막의 모세관현상에 의해 계속 이동하다가 검사점에 이르면 검사점의 또 다른 종류의 SEB 항체에 포획되어 1차 항체-SEB-2차 항체-금입자의 고리를 형성하고, 금입자로 인해 육안으로 식별 가능한 붉은색 점을 형성하였다. 시료용액의 계속적인 이동에 따라 SEB와 반응하지 않은 SEB 항체-금입자는 컨트롤점 방향으로 계속 이동하였고, 컨트롤점의 anti-rabbit 항체와 결합하여 또 하나의 붉은색 점을 생성하였다. 반응을 마친 시료용액은 니트로셀룰로오스 막을 따라 흡수패드 쪽으로 이동하여 흡수패드에 저장되었다.
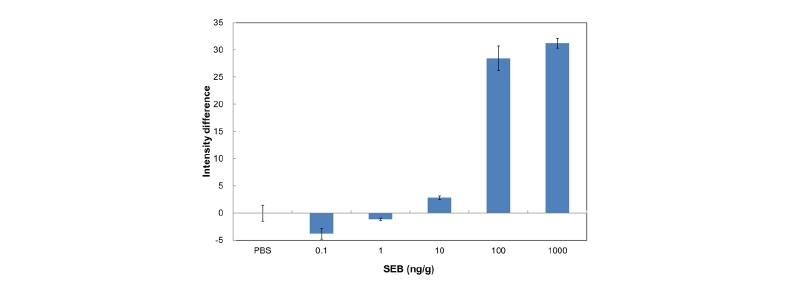
실험 결과 Fig. 2와 같이 SEB의 농도 증가에 따라 검사점에 포획되는 SEB-SEB 항체-금입자 결합물의 양이 증가하여 색이 점차 짙어졌다. SEB의 농도가 100 ng/g일 때부터는 육안으로 쉽게 구분할 수 있을 정도로 검사점의 색이 진해졌다. 영상분석에 의해 계산된 검출한계의 밝기 차이값은 4.41이었으며, 이 값 이상을 나타내는 가장 작은 SEB 농도는 100 ng/g (밝기 차이값, 28.5)인 것으로 조사되었다.
셀룰로오스입자를 표지물질로 하는 진단키트를 이용한 SEB 검출
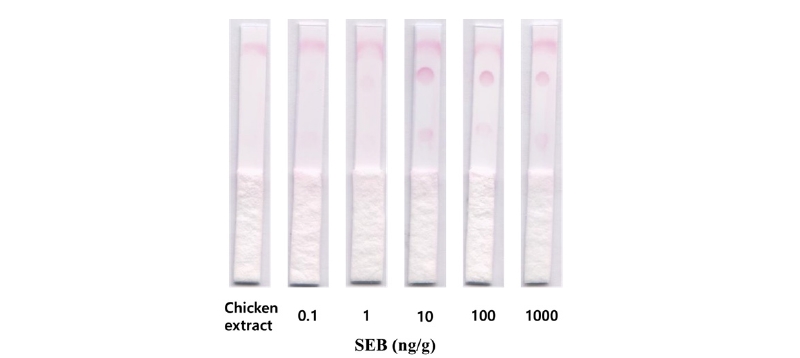
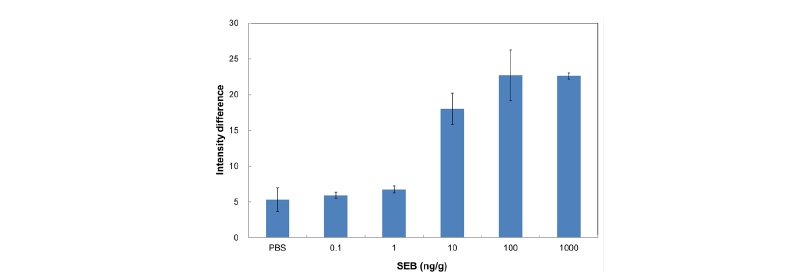
검출 성능을 향상시키기 위해 셀룰로오스입자를 표지물질로 사용한 진단키트의 검사 결과는 Fig. 3의 영상과 같이 밝은 붉은색을 띄었으며, 시료에 포함된 SEB의 농도가 높을 수록 검사점의 색이 짙어지는 경향을 나타냈다. 인산완충 용액에 들어있는 SEB를 검출한 실험 결과 Fig. 4와 같이 금입자를 표지물질로 사용한 진단키트의 SEB 검출 결과(Fig. 3) 보다 낮은 SEB의 농도인 10 ng/g에서 급격한 색 변화를 나타내었다. 영상분석에 의해 계산된 검출한계의 밝기 차이값은 10.4였으며, 이 값 이상을 나타내는 가장 작은 SEB 농도는 10 ng/g (밝기 차이값, 18.0)인 것으로 조사되어 금입자를 표지물질로 사용한 진단키트보다 검출한계를 10배 이상 크게 향상시킬 수 있는 것으로 나타났다. 이러한 검출성능 향상은 셀룰로오스입자의 크기(300 - 400 nm)가 금입자(40 nm)의 크기 보다 커서 눈에 더 잘 띄는 색변화를 일으키기 때문인 것으로 판단된다.
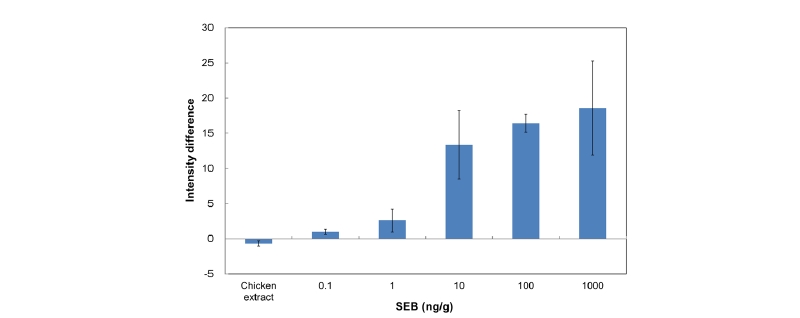
간이 진단키트의 식품시료 적용 가능성을 조사하기 위하여, 닭고기 세척 버퍼에 103 - 10-1 ng/g의 농도로 희석한 SEB를 이용하여 검출 실험을 수행한 결과는 Fig. 5와 같다. 닭고기 세척 버퍼를 이용한 간이 진단키트의 SEB 검출 실험 결과도 인산완충 용액에서의 SEB 검출 실험과 마찬가지로, 시료에 포함된 SEB에 의해 검사점의 색변화를 일으켰으며 농도 증가에 따라 검사점의 색이 짙어지는 경향을 나타냈다. 닭고기 시료에 포함된 여러 가지 다른 물질들의 간섭으로 인한 검출 성능 저하는 나타나지 않았으며, 오히려 인산완충 용액의 경우보다도 잡음신호가 없이 검출 신호가 더 선명하게 나타나는 것으로 조사되었다. 인산완충 용액 시료에서 SEB가 포함되지 않은 대조구의 밝기차이 평균값은 5.3이었으나, 닭고기 세척 버퍼 시료를 이용한 검출실험에서 대조구의 밝기차이 평균값은 - 0.7로 주위 배경과 구분되는 검사점의 색변화를 찾아볼 수 없었다. 이러한 결과는 닭고기 세척 버퍼에 들어있는 어떤 성분이 진단키트 검사점의 비선택적 반응을 감소시킨 때문인 것으로 보인다. 이 때문에 Fig. 3에서 보듯이 닭고기 세척 버퍼에 든 SEB의 농도가 1 ng/g일 때 희미하지만 검사점의 윤곽을 확인할 수 있었다.
영상분석에 의해 계산된 검출한계의 밝기 차이값은 1.2였으며, 이 값 이상을 나타내는 가장 작은 SEB 농도는 1 ng/g (밝기 차이값, 2.6)인 것으로 조사되어 인산완충 용액 시료에서보다 더 낮은 검출한계로 SEB를 검출할 수 있는 것으로 나타났다.
본 연구에서 개발된 셀룰로오스입자를 이용한 진단키트의 SEB 검출 결과는 금입자를 이용한 기존 연구에서의 검출실험 결과인 10 ng/g (Gholamzad et al., 2015)보다도 우수한 것으로 나타났다. 식중독 증상을 일으키는 황색포도상구균 독소의 최소량은 100 - 1 µg/g 정도인 것으로 알려져 있으며(MFDS, 201), 개발된 진단키트의 검출한계는 식품에 포함된 SEB를 식중독을 일으키는 양 이하로 검출 가능한 것으로 조사되었다.
셀룰로오스 나노입자의 가격은 금입자와 차이가 없어 추가 비용을 들이지 않고도 성능이 더 우수한 진단키트를 제작할 수 있을 것으로 기대된다. 또한, 금입자는 하나의 색만을 나타내지만 셀룰로오스 나노입자는 붉은색, 파란색, 녹색 등 다양한 색들이 있어 복수의 검출 대상물을 동시에 검사하는 것도 가능하다. 이러한 진단키트는 외식업체, 대량급식소 등에서 신선도가 의심스러운 식품 재료를 사전 검사하거나, 식중독 사고가 발생하였을 때 원인물질을 파악하여 신속한 조치를 취하는데 활용할 수 있을 것으로 기대된다.
진단키트의 선택성 구명
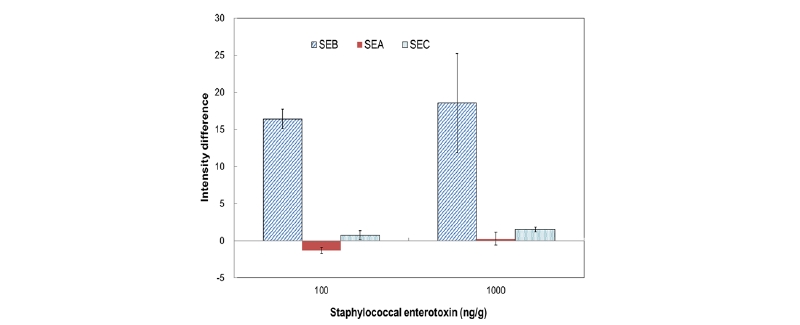
SEB 검출용 간이 진단키트의 검출 대상이 아닌 다른 독소에 대한 반응을 조사하기 위해 검출 대상과 유사한 황색포도상구균 독소 A (SEA) 및 황색포도상구균 독소 C (SEC)를 닭고기 세척액에 희석한 시료를 이용하여 검출 실험을 수행하였다.
실제 식품 시료에 희석한 SEA 및 SEC를 이용한 선택성 실험 결과는 Fig. 6과 같이 SEB용 간이 진단키트에는 이들 독소들이 거의 검출되지 않는 것으로 나타났다. 각 황색포도상구균 독소 농도가 1,000 ng/g일 때 SEC가 미세하게 검출되었으나, SEB와의 밝기 차이값이 12배 이상인 것으로 나타나 개발된 진단키트가 황색포도상구균 독소 B만을 선택적으로 검출함을 확인하였다.
Conclusion
본 연구는 대표적인 식중독 원인물질인 황색포도상구균 독소를 간편하고 빠르게 검사할 수 있는 간이 진단키트를 개발하기 위하여 수행되었다. 간이 진단키트는 니트로셀룰로오스막의 모세관현상을 이용하는 측방유동형을 이용하였으며, 독소의 오염에 따라 색변화를 일으키는 표지물질로는 많이 사용되어져 왔던 금입자와 검출 성능을 향상하기 위한 목적으로 셀룰로오스입자를 사용하였다. 개발된 간이 진단키트의 황색포도상구균 독소(SEB) 검출 성능은 인산완충 용액 또는 닭고기 세척액에 농도별로 희석한 표준 SEB를 이용하여 조사하였다. 이러한 연구결과를 요약하면 다음과 같다.
첫째, 금입자를 표지물질로 이용한 간이 진단키트의 SEB 검출한계는 100 ng/g인 것으로 나타났다.
둘째, 셀룰로오스입자를 표지물질로 이용한 간이 진단키트의 SEB 검출한계는 인산완충 용액 및 닭고기 세척액 시료에 대하여 각각 10 ng/g 및 1 ng/g로 나타났다. 셀룰로오스 입자를 표지물질로 사용하였을 때 금입자를 표지물질로 사용하였을 때보다 검출성능이 향상되었으며, 개발된 간이 진단키트로 식중독을 일으키는 SEB의 최소량보다 작은 농도의 독소를 검출할 수 있는 것으로 조사되었다.
셋째, 개발된 SEB용 진단키트는 SEA 및 SEC와 같은 유사 독소에 의한 교차반응 없이 황색포도상구균 독소 B만을 선택적으로 검출하는 것으로 나타났다.