Introduction
현대의 작물 생산을 위한 기술은 합성 농약 및 비료에 크게 의존적이고, 인구의 증가, 생활수준의 향상과 함께 식량 수요가 점점 크게 증가하고 있다. 이러한 증가는 결국 토양의 물리화학적 변화와 토양과 물의 오염 등을 일으켜 지구 생태계의 생물다양성에 심각한 피해를 주고 있다. 따라서, 이러한 문제를 해결하고 지속적 농업의 목적을 달성하기 위해 작물의 품종개량, 토양의 비옥도 증진 등 작물 보호와 재배 체계에 대해 연구가 필요하나 가장 걸림돌이 되고 있는 것 중의 하나는 잡초의 방제이다. 이러한 잡초는 전세계적으로 약 1,800여 종이 있고, 이 중 주요 잡초는 200여종이 알려져 있다(Kim et al., 2020). 이와 같이 잡초에 의한 피해는 농업생산 시 재해 손실의 약 30%를 차지하여 병충해 및 토양 손실과 함께 4대 농업 재해의 하나이다.
천연물을 이용한 해충방제는 많은 연구성과가 이루어져 상용화(Cremlyn, 1991)되었으나, 생물학적 잡초 방제의 예는 많지 않다. 현재에는 곰팡이만이 생물학적 방제의 도구로서 이용되고 있는데, 상용화된 미생물 제초제로는 감귤의 stranglervine (Morrenia odorata)의 방제에 역병균(Phytophthora plamivora)의 포자 현탁액, 벼와 대두 재배지의 서양자귀풀(northern jointvetch, Aeschynomene virginica)의 방제를 위해 탄저병균(Colletotrichum gleosporioides Sacc. f. sp.)의 건조분말제제가 사용되고 있으며, 여러 가지 주요 잡초를 방제하기 위해 여러 병원균의 개발이 추진 중에 있다(Watson, 1989). 또한 제초제로 이용할 수 있는 다양한 천연물 계열로 상호대립억제물질(allelochemicals)을 생각할 수 있다(Francisco et al., 1999; Chou, 2000). 이러한 화합물들은 식물에 의해 인접한 환경으로 분비되는데, 다른 식물의 생장을 지연시키거나 억제하여 주어진 환경에서 경쟁력을 획득하게 된다. 이러한 상호대립억제력을 가진 화합물들은 식물에 존재하며 휘발, 뿌리로부터의 삼출, 용탈 또는 식물 잔해의 분해 과정 등에 의해 분비될 수 있다. 상호대립 억제물질의 후보물질로는 독성가스, 유기산과 알데히드, 방향족산, 불포화 락톤, 쿠마린, 플라보노이드, 탄닌, 알칼로이드, 테르페노이드, 스테로이드 등을 들 수 있다. 이러한 상호대립억제물질은 식물에서의 여러 가지 2차 대사산물 중 한 가지 예로 이들 대부분의 생물학적 특성은 알려져 있지 않다. 식물계에서 약 40만 가지의 2차 대사산물이 합성되고 있을 것으로 추정하고 있으며(Cremlyn, 1991), 이러한 다양한 화학구조를 가진 여러 가지 화합물을 제초제 개발을 위한 선도 물질로 이용할 수 있을 것으로 생각하고 있다. 본 연구에서는 식물체 유래의 제초활성 성분을 탐색하기 위하여 200여종의 식물추출물을 이용하여 screening을 실시하였다. 이중 강한 활성을 가지며 아직 많은 연구가 이루어진 바 없는 곤달비(Ligularia stenocephala M.)를 재료로 하여 활성물질을 분리·정제하고 화학구조를 구명하였기에 보고하고자 한다.
Materials and Methods
재료 및 시약
곤달비는 강원도 평창의 농가로부터 구입하여 실험에 사용하였다. 종자소독제는 프로라츠 유제(Spotack EC, Korea Samgong, Seoul, Korea)를, Tween 20은 Tokyo Kasei (Tokyo, Japan) 사의 제품을 사용하였다. Chloroform (CHCl3), ethyl acetate (EtOAc), methanol (MeOH), butanol (n-BuOH) 및 n-hexane 등 용매는 삼전순약(Samchun pure chemical Co., Ltd., Seoul, Korea) 제품을 사용하였다. HPLC용 formic acid, silica gel (70 - 230 mesh), TLC plate (20 × 20 cm, 0.25 mm layer thickness, Kieselgel 60GF 254)는 Merck (E. Merck, Damstadt, Germany)사 제품을 사용하였고, 그 외의 HPLC용 시약은 국내산 공업용 시약을 정제하여 사용하였다. Nuclear magnetic resonance (NMR) 용매 CDCl3와 Sephadex LH-20은 Sigma-Aldrich (St Louis, MO, USA) 제품을 사용하였다.
기기
NMR spectrometer는 Bruker DMX 600 (600 MHz, Bruker Analytische Messtechnik, Rheinstetten, Germany)을 이용하여, tetra methyl silane (TMS)를 내부표준물질로 사용하였고, chemical shift는 ppm (δ)으로 나타내었다. High performance liquid chromatography (HPLC)는 LC900 (JASCO, Tokyo, Japan), electron ionization mass spectrometry (EI-MS)는 Hitachi M-80A (Hitachi, Tokyo, Japan), U-IS Spectrometer는 UV-1601 UV-Vis spectrophotometer (Shimadzu, Kyoto, Japan)를 사용하였다.
제초 활성 검정
논피(Echinochloa crus-galli)는 한국화학연구소 생물검정실험실로부터 분양, 상추(Lactuca sativa L.)는 종자상에서 구입, 메벼(Oryza sativa L.)는 충남대학교 부속농장에서 채집하여 사용하였다.
제초 활성 물질의 검색
저온수(4℃)에서 2개월 저온 처리된 논피, 벼, 그리고 상추 종자를 증류수 100 mL에 종자소독약인 스포탁 유제 50 μL를 희석 한 후 24시간 동안 침지시켰다. 종자를 수세하여 petri-dish에 여지(3M paper)를 깔고 증류수를 첨가한 다음 incubator (25℃, 상대습도 70%, 4200 Lux)에서 3일간 생장시켰다. 각각의 petri-dish에 여지(3M paper, ϕ 9 cm)를 깔고 0.5% aqu. Tween 20으로 추출물을 1000, 200, 100, 20, 10 ppm이 되도록 희석하여 petri-dish 당 6 mL씩 가하였다. 정제된 단일 물질은 0.5% aqu. Tween 20으로 stock solution을 10-2, 10-3, 10-4, 10-5 M이 되도록 희석하여 petri dish (ϕ 3 cm)에 가하였다. 발아된 종자의 뿌리 길이가 약 5 mm정도 되는 것을 골라 petri dish당 9립씩 옮겨 incubator에서 생장시켰다. 일주일 경과 후, 무처리구 대비 추출물 처리구에 대한 검정 식물의 뿌리 길이를 측정하여 저해율을 구하였다.
 (1)
(1)
제초 활성 물질의 분리
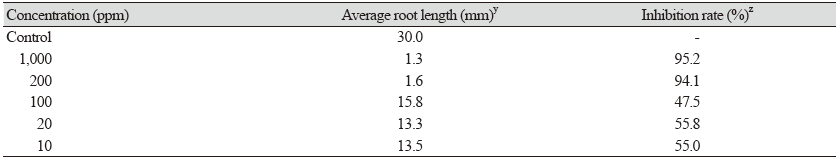
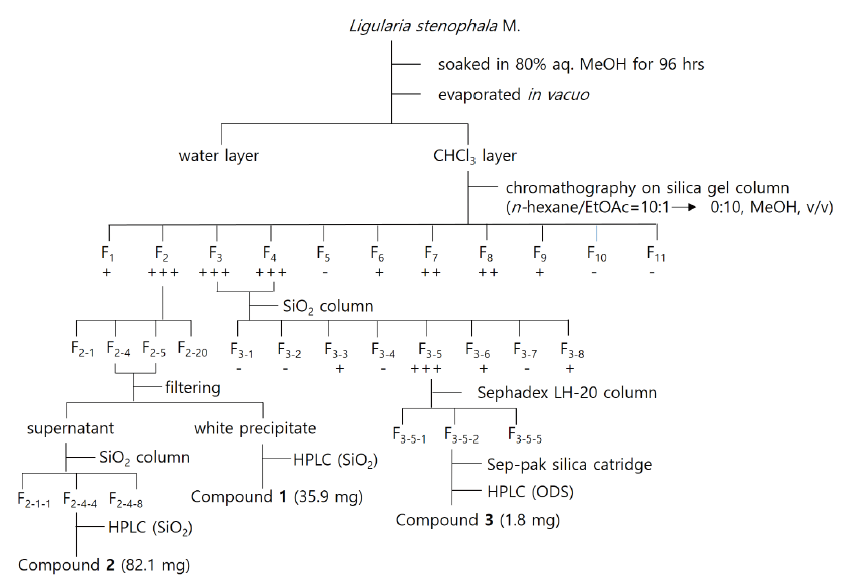
음건한 후 마쇄한 곤달비 잎 분말(4 kg)을 80% (v/v) aqu. MeOH 72 L에 약 96 시간 침지한 후 감압 여과하였다. 여액은 감압농축한후 증류수를 가하고 동량의 CHCl3, EtOAc, n-BuOH 순으로 분획하였다. 활성검정 결과 CHCl3층과 EtOAc층에서 강한 제초활성을 나타내어(Table 1), 양도 많고 높은 활성을 가진 CHCl3층(35.8 g)을 이용하여 활성물질의 분리를 실시하였다. 1차 silica gel column chromatography (1.5 kg, 6 × 100 cm, n-hexane/EtOAc = 10 : 0 → 0 : 10, MeOH, v/v)를 실시하여 11개의 분획(F1~11)을 얻었다. 이중 F2층(6.08 g)을 2차 silica gel column chromatography (n-hexane/EtOAc = 10 : 0 → 0 : 10, MeOH, v/v) 를 실시하여 20개의 분획(F2-1~20)을 얻었다. 이어서 F2-4층 (1.561 g)으로부터 얻은 백색 침전물 (50 mg)을 prep-HPLC (Develosil 30 - 10/20, silica, 20 × 250 mm, n-hexane/EtOAc = 1 : 1, v/v)로 정제하여 Compound 1 (35.9 mg)을 분리하였다. 또한, 여액(1.51 g)을 3차 silica gel column chromatography (n-hexane/EtOAc = 15 : 1, MeOH, v/v)를 실시하여 8개의 분획(F2-4-1~8)층을 얻었다. 이 중에서 F2-4-4층 (385 mg)을 Prep-HPLC (silica, n-hexane/EtOAc = 4 : 1, v/v)을 이용하여 Compound 2 (82.1 mg)를 분리하였다. 두 번째로 활성이 높은 F3 - F4층 (5.28 g)을 2차 silica gel column chromatography (CHCl3/acetone/formic acid = 9 : 1 : 0.1, MeOH, v/v/v)를 실시하여 8개의 분획층(F3~8)을 얻었다. 이 중에서 활성이 높은 F3-5층(1.615 g)을 Sephadex LH-20 column chromatography (CHCl3/MeOH = 1 : 1, v/v)를 실시하여 5개의 분획(F3-5-1~5)층을 얻었고, 활성이 높은 F3-5-2층을 다시 Sep-pak silica cartridges (n-hexane, CHCl3, EtOAc, MeOH) 로 분리하였다. 이 중에서 활성이 높은 CHCl3층(192 mg)을 prep-HPLC (octadecyl silica, 20 × 250 mm, 55% aq. acetonitrile)를 이용하여 Compound 3 (1.8 mg)을 분리하였다(Scheme 1).
Results and Discussion
제초 활성 검정
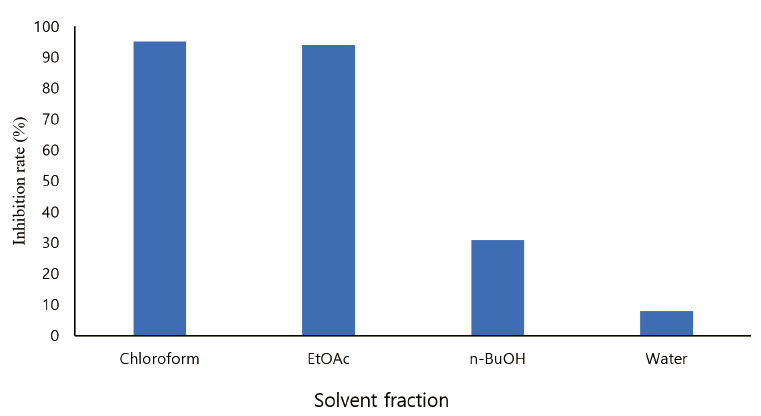
논피에 대한 제초활성검정을 실시한 결과, 곤달비 잎의 CHCl3층과 EtOAc 층에서 각각 95.2%와 94.1%로 높은 활성을 나타냈다(Fig. 1).
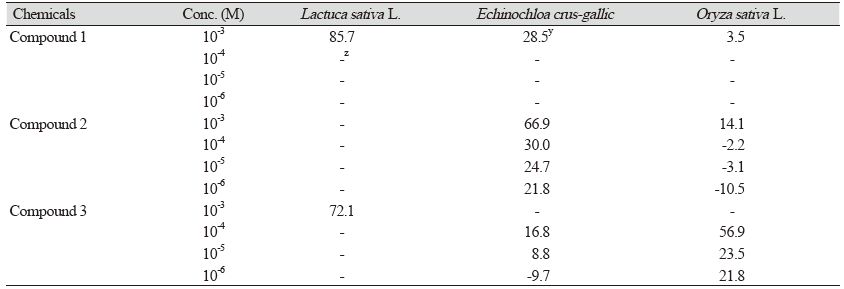
곤달비로부터 분리된 euparin, 5,6-dimethoxy-2-isopropenylbenzofuran, liguhodgsonal에 대한 제초활성 검정 결과, euparin은 10-3 M에서 광엽식물인 상추에 대해 높은 제초활성을 나타냈으나, 화본과 식물인 논피와 벼에 대해 낮은 활성을 나타냈다. 5,6-dimethoxy-w-isoprophenyl benzofuran은 10-3 M에서 벼보다 논피에 더 강한 제초활성을 보였다. 반면 liguhodgsonal은 euparin과 마찬가지로 상추에서 높은 활성을 나타냈으며 10-4 M에서 논피보다 벼에 더 활성을 나타냈다(Table 2). 이상의 결과로 볼 때, euparin은 상추에 대해, 5,6-dimethoxy-2-isopropenylbenzofuran, liguhodgsonal은 화본과 식물인 논피와 벼에 대해 선택적 활성을 나타내었다. 향후 유근 신장 저해 활성 이외에 경엽처리에 의한 활성 검정 및 작용 기작에 관한 연구도 수행되어야 할 것으로 사려된다.
제초활성물질의 구조결정
Compound 1
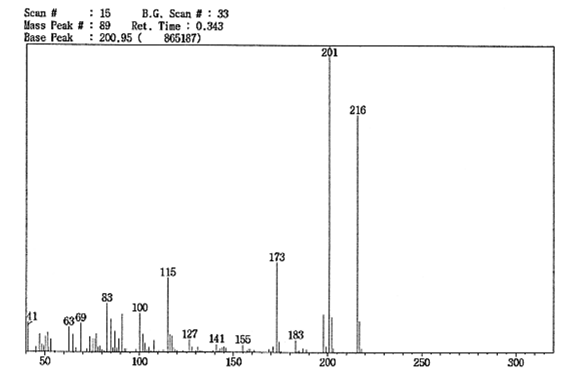
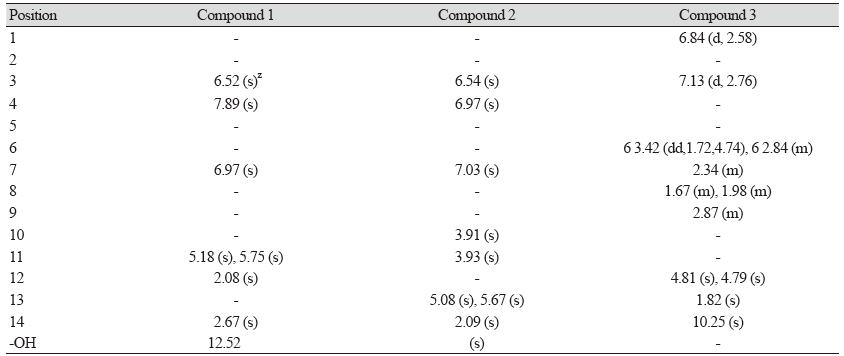
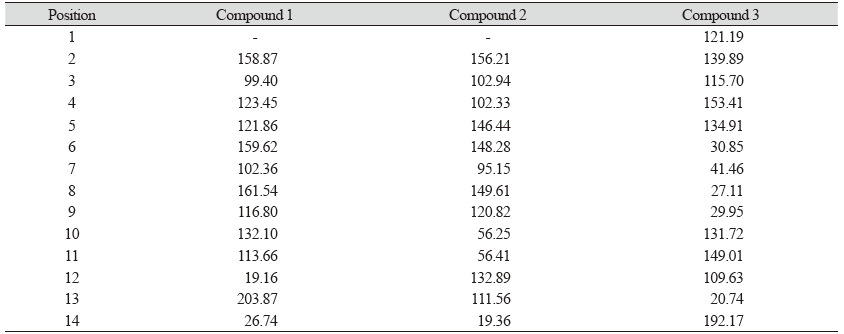
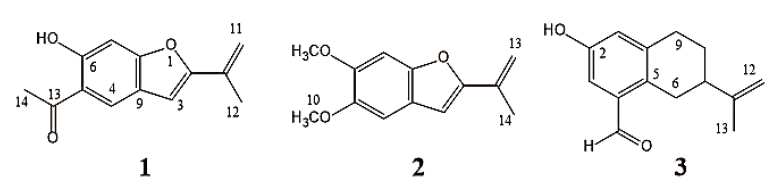
Compound 1은 노랑색 분말로 얻어 졌으며 silica gel TLC 상에서의 Rf값은 0.63 (n-hexane/EtOAc = 1 : 1, v/v), UV-Vis spectrum은 395.5 nm에서 최대 흡수치를 나타내었다. EI-MS 측정결과, 분자이온 peak가 m/z (M+) 216으로 나타났으며, 201 (M-CH3)+, 173 (M-COCH3)+를 갖는 fragment peak가 확인되어 methyl group과 acetyl group이 존재함을 알 수 있었다(Fig. 2). 1H-NMR spectrum에서, methyl proton peak가 2.08, 2.67 ppm에서 각각 singlet, methylene group의 proton peak가 5.18, 5.75 ppm에서 각각 singlet으로 확인되었다. 6.97, 7.89 ppm에서 aromatic ring 2개의 proton peak가 singlet, 6.52 ppm에서 1개의 methine proton peak, 12.52 ppm에서 hydroxyl proton peak가 singlet으로 확인되었다(Table 3). 13C-NMR spectrum에서 13개의 carbon signal이 확인되었다. 203.87 ppm에서 ketone carbon signal, 116.80 - 161.54 ppm 사이에서 aromatic methine 및 quaternary carbon peak가 관측되었다(Table 4). 이상의 기기 분석 결과를 종합하여 분자식은 C13H12O3, 분자량이 216인 euparin으로 동정하였다.
Compound 2
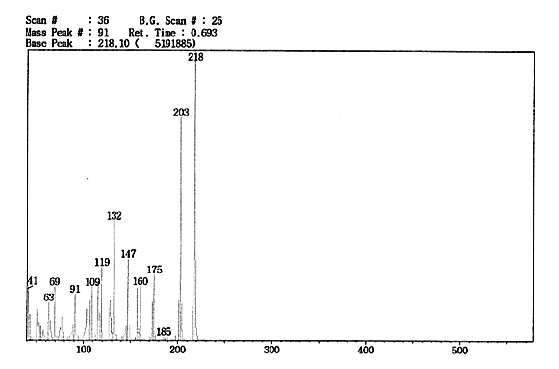
Compound 2는 노랑색 분말로 얻어 졌으며 silica gel TLC 상에서의 Rf값은 0.33 (n-hexane/EtOAc = 4 : 1, v/v)이었다. EI-MS의 molecular ion peak가 m/z 218에서 관찰되어 이 화합물의 분자량은 218임을 확인하였다. 또한, fragment ion peak가 m/z 203 (-CH3), 175 (M-OCH3), 160 (M-OCH3-CH3)에서 관측되어 methyl group과 methoxy group이 존재함을 알 수 있었다(Fig. 3). 1H-NMR spectrum을 해석한 결과, compound 1의 1H-NMR spectrum에서 관측되었던 carbonyl group에 결합되어 있는 methyl group의 signal과 OH의 proton signal이 검출되지 않았고, 두개의 methoxy signal이 관찰된 것 외에는 매우 유사한 양상을 나타내었다. 이것으로 보아 compound 2는 compound 1과 유사한 화학구조를 갖는 화합물일 것으로 추정하였다. 2.09 ppm에서 methyl proton signal, 5.08, 5.67 ppm에서 methylene group의 2개의 proton이 각각 singlet으로 확인되었다. 3.91, 3.93 ppm에서 methoxy proton peak, 6.54 ppm에서 1개의 methane proton peak가 singlet으로 확인되었다(Table 3). 13C-NMR spectrum에서 13개의 carbon peak가 관찰되었고, 56.25, 56.41 ppm에서 2개의 methoxy carbon peak가 각각 확인되었다. 95.16 - 149.61 ppm 사이에서 6개의 aromatic carbon peak가 확인되었다(Table 4). 이상의 기기 분석결과로부터 분자식 C13H14O3, 분자량 218인 benzenoid계의 5,6-dimethoxy-2-isoprophenyl benzofuran으로 동정하였다(Fig. 4).
Compound 3
Compound 3은 백색 분말로 얻어졌으며, silica gel TLC 상의 Rƒ값은 0.68 (n-hexane/EtOAc = 1 : 1, v/v)이었다. EI-MS spectrum 해석 결과 m/z 216에서 분자 이온 peak, m/z 201 (M-CH3), 188 (M-CO), 173 (M-CO-CH3)에서 fragment ion peak가 관측되었다. 1H-NMR을 측정한 결과 1.82 ppm에서 methyl proton peak가 singlet, 4.79, 4.82 ppm에서 methylene proton peak, 6.84, 7.13 ppm에서 aromatic methine proton peak (d, 1H, J = 2.4 Hz), 10.25 ppm에서 aldehyde proton peak가 singlet으로 관찰되었다. 2.84 ppm에서 3개의 proton peak가 겹쳐서 multiplet, 3.41 ppm에서 proton peak (dd, 1H, J = 4.62, 4.74 Hz)가 확인되었다(Table 3). 13C-NMR spectrum을 해석한 결과 20.74 ppm에서 methyl carbon peak, 109.63 ppm에서 methylene carbon peak가 각각 확인되었다. 120 - 160 ppm 사이에서 6개의 aromatic carbon peak, 25 - 45 ppm 사이에서 3개의 methylene carbon peak와 1개의 methine carbon peak, 192.17 ppm에서 carbonyl carbon peak가 확인되었다(Table 4). 이상의 결과를 종합하여 분자식은 C14H16O2, 분자량은 216인 norsesquiterpenoid계인 liguhodgsonal로 동정하였다(Fig. 4).
Conclusions
곤달비의 각 부위별로 제초활성검정을 한 결과, 곤달비 잎의 chloroform 층과 EtOAc층이 논피에 대해 1,000 ppm에서 각각 95.2, 94.1%로 높은 유근 저해 활성을 나타났다. 이 중 chloroform 층을 농도별로 활성 검정한 결과, 10 ppm에서도 50% 이상의 제초활성을 나타내어 활성물질의 분리를 실시하여 3종의 화합물을 분리하였다. EI-MS, 1H-NMR, 13C-NMR 등 기기분석을 이용하여 화학구조를 분석한 결과, benzenoid계인 euparin, 5,6-dimethoxy-2-isoprophenylbenzofuran과 norsesquiterpene계인 liguhodgsonal로 각각 동정되었다. Euparin은 10-3 M에서 상추에 대해서만 선택적으로 제초활성을 보였고, 5,6-dimethoxy-2-isoprophenylbenzofuran 및 liguhogsonal은 화본과 식물인 벼와 논피에 대해서 선택적 활성을 보였다. Euparin과 5,6-dimethoxy-2-isopropenylbenzofuran은 Murae et al. (1968)에 의해 구조가 밝혀졌고, Patula에서도 분리 동정(Sutfeld et al., 1985) 되었으며, Liguhodgsonal은 Senecio 속(Bohlmann and Ziesche, 1981)과 L. veitchiana (Zhao et al., 1994)에서도 분리·동정되었다. 이들 화합물의 제초활성에 대한 보고는 이번이 처음이다.