Introduction
작물의 성장 과정에서 질소(N, nitrogen)는 필수적인 다량 원소 중 하나이며, 작물 내에서 단백질과 엽록소 합성에 중요한 요소이다(Meng et al., 2017; Jung et al., 2020). 재배 기간 중 질소 결핍은 작물의 양분 불균형을 초래하며, 과도한 질소 공급은 작물의 수분 및 질소이용효율을 낮추고, 질소 용탈을 일으키며, 작물의 과도한 성장을 유발하여 품질을 저하시킨다고 보고되었다(Kim et al., 2007; Bassi et al., 2018; Xu et al., 2019). 이러한 이유로 인해 작물의 수량 증대 및 품질 향상을 포함하는 지속 가능한 농업을 위해 질소 시비량 개선 등의 효율적인 관리 방안이 필요하다. 토양에 투입된 질소의 대부분은 작물 생육에 사용되지만 투입된 질소의 약 10 - 20%는 탈질 과정에 의해 암모니아(NH3) 또는 아산화질소(N2O)와 같은 가스 형태로 휘산된다(Allison, 1966; Kundler, 1970). 특히 2016년 기준 국내 농업부문 NH3 총 배출량은 전체 NH3 총 배출량의 약 78.7%에 해당하는 237,017 톤이 배출되었다(NIER, 2019). 토양에서 발생한 NH3는 대기 중에 존재하는 질소산화물(NOx)이나 황산화물(SOx)과 반응하여 질산암모늄(NH4NO3)과 황산암모늄(NH4SO4) 등의 2차 미세먼지를 생성한다(Anderson et al., 2003). 또한 NH3는 악취를 유발하고, 토양과 작물 사이에서 양분의 불균형을 일으키며, 자연생태계 및 생물다양성에 큰 영향을 미친다(Gundersen and Rasmussen, 1990; Bobbink et al., 1992; Asman, 1994).
NH3는 농업부문에서 주로 가축분퇴구비 및 비료 사용에 의해 배출되며, 토양 내에서 NH4+가 OH-와 결합하면서 배출된다(Lim et al., 2012). 그로 인해 농업부문에서는 환경으로 배출되는 NH3를 저감을 목적으로 황산알루미늄을 이용해 토양의 pH를 7 이하로 낮추거나, 무기질비료를 대신하여 유기질비료를 사용하는 등 다양한 방법을 제시 및 개발하였다(Wang et al., 2016). 하지만 대부분의 방법들이 경제성이 낮고, 다른 오염을 유발할 수 있기에 현실적으로 적용이 매우 어려운 실정이다(Guo et al., 2019). 그에 따라 적용이 용이하며, 경제적으로 농경지 토양에서 발생하는 NH3를 저감시킬 수 있는 새로운 방안이 필요한 실정이다.
바이오차(biochar)는 바이오매스(biomass)와 숯(charcoal)의 합성어로 다양한 부산물을 산소가 제한된 조건에서 열 분해한 탄소 함량이 높은 고형물질이다(Sohi, 2010; Oh et al., 2017; Lee et al., 2019; Hong et al., 2020). 바이오차는 토양에 처리되었을 때 토양의 pH 조절, 물 유지 능력 증가, 미생물 주거지 제공 등 다양한 특성에 의해 농업 생산성을 향상시킬 수 있다(Woo, 2013; Lee et al., 2018). 바이오차 처리에 따른 농업 생산성 증가 효과는 산성토양과 같은 척박한 토양에서 연구를 수행함으로서 입증되었다(Crane-Droesch et al., 2013). 바이오차는 다양한 물질을 흡착하는 미세공극을 가지고 있어 흡착을 통한 NH3를 포함한 다양한 오염물질 및 중금속을 저감·제거시키는 수단으로 활용이 가능하다(Park et al., 2020). 이외에도 토양의 유기탄소를 증가시키고, 온실가스를 저감하는 능력으로 인해 세계적으로 주목받고 있는 친환경소재이다(Lehmann et al., 2008; Han et al., 2011). 바이오차 제조를 위해 왕겨를 사용하였으며, 왕겨는 국내에서 2번째로 많이 발생하는 농업 부산물이며, 매년 약 114만 6,800 톤이 발생하고 있다(NAAS, 2012).
따라서 본 연구는 매년 대량으로 발생하는 왕겨를 환경친화적으로 재활용할 수 있는 방안 중 하나인 바이오차를 활용하여 무기질비료를 시비한 토양에 pH가 다른 바이오차를 처리했을 때 바이오차에 의한 NH3 저감 효율을 평가하고자 하였다.
Materials and Methods
공시 재료
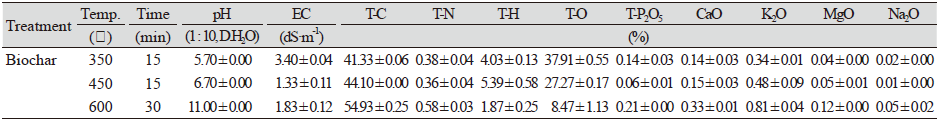
실험에 사용된 토양은 충남대학교 농업생명과학대학 부설 시험포장에서 채취하여 유리온실에서 2주간 풍건 후 2 mm 이하로 체거름하여 사용하였다. 바이오차는 pH에 따라 산성(pH 5.7), 중성(pH 6.7), 알칼리성(pH 11.0) 바이오차로 구분하기 위해 조건을 달리하여 제조한 바이오차를 푸른네이처(Purnnature, Suncheon, Korea)와 유기산업(Yoogi Industry, Gochang, Korea)에서 구매하여 이용하였다. 실험에 사용된 토양과 바이오차의 화학적 특성은 Table 1과 2에 나타내었다.
처리구 설정
처리구는 무처리구(control), 대조구(N), 바이오차처리구(BC + N)로 설정하였다. 비료는 노지 배추의 시비처방기준에 준하여 요소(Urea, N), 용성인비(P2O5), 염화칼륨(K2O)를 시비하였다. NH3 배출에 직접적인 영향을 주는 요소는 반량(160 kg·ha-1), 기준량(320 kg·ha-1), 배량(640 kg·ha-1)으로 구분하여 처리하였으며, 용성인비와 염화칼륨은 모든 처리구에 동일한 양을 처리하였다. 바이오차는 pH (pH 5.7, 6.7, 11.0)에 따라 토양의 중량 대비 1% (w·w-1)으로 처리하였으며, 실험 기간 중 토양의 수분함량은 매일 증류수를 첨가하여 20%로 유지하였다.
NH3 배출량 평가
NH3 배출량 평가는 dynamic column을 이용하였다. Column은 아크릴을 이용하여 제작하였으며, 내부 크기는 90 cm (Ø) × 50 (H) cm이다. NH3 포집은 매일 오전 9시에 0.05 N H2SO4으로 포집하였다. 포집한 NH3 시료는 Indophenol blue 비색법을 이용하여 640 nm에서 분광광도계(GENESYS 50 UV-Vis spectrophotometer, Thermo Scientific Inc., Waltham, Massachusetts, USA)를 이용하여 비색정량하였다.
NH3 배출량을 계산한 계산식은 다음과 같다.
J = Q / AL × ((C × V) / (Q × t) × R) × 10 (1)
J, NH3-N flux (g·ha-2·min-1);
Q, 시료채취 기간 동안 유량(m2·min-1);
AL, chamber 내 headspace의 면적(m2);
C, chamber 내의 NH3-N의 농도(μg·m-2);
V, 포집액의 용량(L);
T, 포집한 시간(min);
R. NH3의 전체 분자량 중 N이 차지하는 비율.
토양 및 바이오차 분석
토양의 화학적 특성은 pH, 전기전도도(EC, electrical conductivity), 총 탄소(T-C, total carbon), 총 질소(T-N, total nitrogen), 유효 인산(Av. P2O5, available phosphate), 치환성 양이온(Ex. cations, exchangeable cations, Ca2+, K+, Mg2+, Na+)을 분석하였다. 토양의 pH와 EC는 토양과 증류수를 1 : 5 (w·v-1)로 혼합하여 30분간 진탕 후 1시간 동안 방치한 혼합액을 pH · EC meter (ORIONTM Versa Star ProTM, Thermo Scientific Inc., Waltham, Massachusetts, USA)를 이용하여 측정하였다. T-C와 T-N는 Element Analyzer (TruSpec Micro, Leco, Michigan, USA)을 이용하여 분석하였다. Av. P2O5는 Lancaster법을 이용하여 720 nm에서 분광광도계(GENESYS 50 UV-Visible spectrometer, Thermo Scientific Inc., Waltham, Massachusetts, USA)를 이용하여 분석하였다. Ex. cations (Ca2+, K+, Mg2+, Na+)는 pH 7.0으로 교정한 1 M NH4OAC로 침출하여 ICP-OES (Inductively Coupled Plasma-Optical Emission Spectrometer, PerkinElmer Avio 500, Thermo Scientific Inc., Waltham, Massachusetts, USA)를 이용하여 분석하였다.
바이오차의 pH와 EC는 바이오차와 증류수를 1 : 10 (w·v-1)로 혼합하여 30분간 진탕 후 1시간 동안 방치한 혼합액을 pH · EC meter (ORIONTM Versa Star ProTM, Thermo Scientific Inc., Waltham, Massachusetts, USA)를 이용하여 측정하였다. T-C, T-N, 총 수소(T-H, total hydrogen), 총 산소(T-O, total oxygen)는 Element Analyzer (TruSpec Micro, Leco, Michigan, USA)을 이용하여 분석하였다. T-P2O5와 Cations (CaO, K2O, MgO, Na2O)는 Nitric acid와 Perchloric – Nitric acid 용액으로 산분해하여 ICP-OES (Inductively Coupled Plasma-Optical Emission Spectrometer, ICAP 7000series ICP spectrometer, Thermo Scientific Inc., Waltham, Massachusetts, USA)로 분석하였다.
통계 분석
통계 분석은 SPSS (IBM SPSS Statistics version 26, IBM SPSS, NY, USA) 일원배치분산분석(ANOVA, ONE way analysis of variance)을 통해 95% 신뢰수준에서 유의성 검정을 수행하였으며, Duncan의 다중 범위 검정(Duncan`s multiple range test)을 통해 각 처리구 사이의 유의차를 확인하였다.
Results and Discussion
NH3 배출량 평가
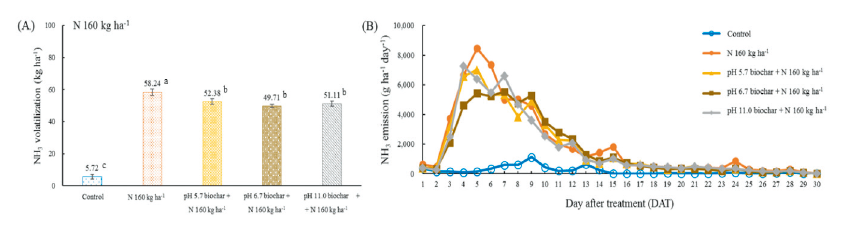
160 kg·N·ha-1를 처리한 처리구의 일별 배출량 변화 추이와 총 배출량을 나타낸 그래프는 Fig. 1에 나타낸 바와 같다. 무처리구를 제외한 모든 처리구에서 DAT (day after treatment) 4 - 5에 일일 최대배출량을 보였으며, 대조구에서 약 8.46 kg·ha-1로 가장 많은 배출량을 보였다. DAT 5 이후 전체적으로 배출량이 감소하였으며, DAT 25에 무처리구(Control)와 유사한 경향을 보였다. 대조구인 N 160 kg·ha-1 처리구의 NH3 총 배출량은 약 58.24 kg·ha-1이었으며, 대조구에 바이오차 처리 시 pH에 따라 각각 약 52.38, 49.71, 51.11 kg·ha-1이었다. pH 6.7 바이오차를 처리한 처리구에서 NH3 배출량이 최대 15% 감소하였으며, 다른 처리구에서도 약 10 - 12% 감소하였다.
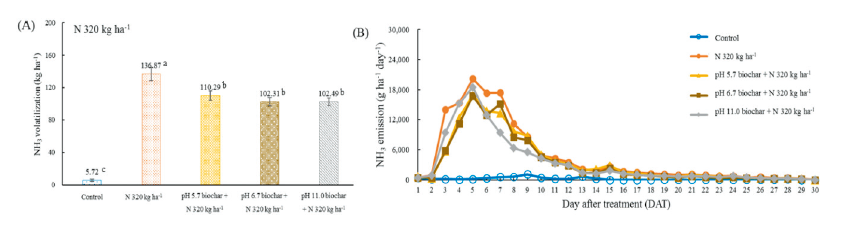
320 kg·N·ha-1를 처리한 처리구의 배출량 변화 추이 및 배출량은 Fig. 2와 같다. 무처리구를 제외한 모든 처리구에서 DAT 5에 일일 최대배출량을 나타냈으며, 대조구에서 약 20.20 kg·ha-1로 가장 많이 배출되었다. DAT 5 이후 모든 처리구에서 배출량이 감소하였으며, DAT 26 이후 무처리구와 유사한 배출 경향을 나타냈다. N 320 kg·ha-1 처리구의 총 배출량은 약 136.87 kg·ha-1이었으며, 바이오차 처리 시 각각 110.29, 102.31, 102.49 kg·ha-1이었다. pH 6.7 biochar + N 320 kg·ha-1와 pH 11.0 biochar + N 320 kg·ha-1의 배출량은 약 25% 감소하였으며, pH 5.7 바이오차 처리 시 NH3 배출량이 약 19% 감소하였다.
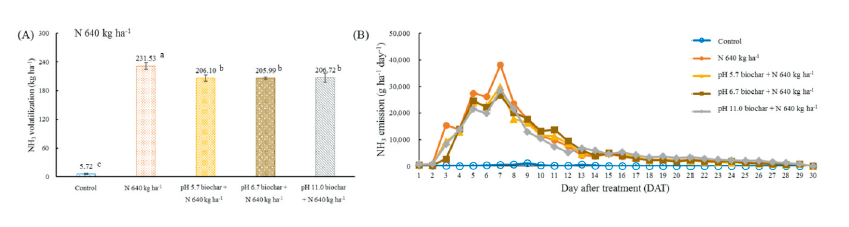
640 kg·N·ha-1를 처리한 처리구의 일별 배출량 변화 추이 및 총 배출량은 Fig. 3와 같다. 무처리구를 제외한 모든 처리구는 DAT 7에 일일 최대배출량을 보였으며, 대조구에서 38.12 kg·ha-1로 가장 많은 배출량을 보였다. DAT 7 이후 배출량이 점차 감소하였다. DAT 29에 무처리구와 유사한 배출량을 보였다. N 640 kg·ha-1 처리구의 총 배출량은 231.53 kg·ha-1이었으며, 바이오차 처리 시 각각 206.10, 205.99, 206.72 kg·ha-1이었다. 바이오차를 처리한 모든 처리구에서 약 11%의 배출량 저감 효과를 보였다. 토양에 요소 시용에 따른 NH3 배출은 Sun 등(2017)의 보고와 유사하게 실험 초반에 매우 빠른 속도로 진행되었다. 바이오차 처리에 따른 NH3 배출량 감소는 다양한 연구를 통해 확인되었으며, 이는 표면의 작용기, pH, CEC, 바이오차의 침투 깊이 등 다양한 인자의 영향을 받는 것으로 보고되었다. 그 중에서도 바이오차 제조 시 열 분해 온도, 바이오차 및 토양의 pH가 가장 밀접한 관련을 갖는다고 첨언하였다(Mandal et al., 2016; 2018; Kim et al., 2021). 또한 요소는 토양 내에서 NH4+형태로 가수분해된 후, NH3로 배출되지 않고 질산화과정을 거쳐 N2O 형태로도 유실될 수 있다(Han and Hong, 2019).
토양의 화학적 특성 평가
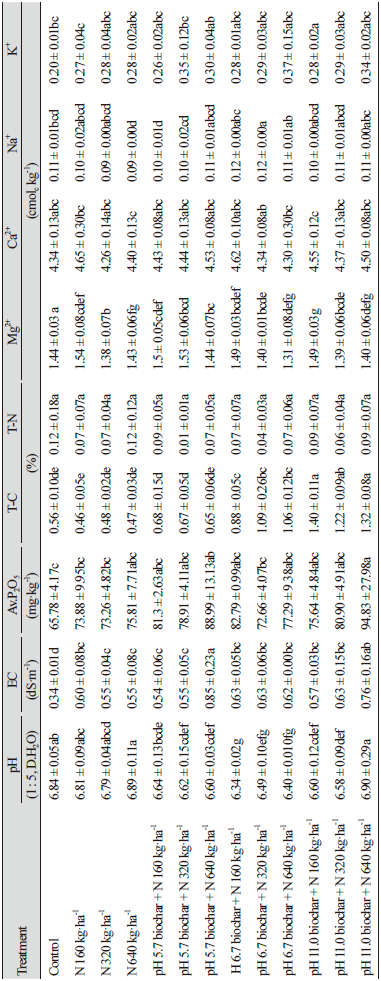
실험 후 토양의 화학적 특성은 Table 3에 나타내었다. 실험 후 토양의 pH는 pH 6.7 biochar + N 160 kg·ha-1 처리구에서 pH 6.34로 가장 낮았으며, pH 11.0 biochar + N 640 kg·ha-1 처리구에서 pH 6.90으로 가장 높았다. 실험 전 토양(pH 6.89)에 비해 실험 후 모든 처리구에서 비슷하거나 감소하였다. 이는 비료 사용으로 인해 토양이 산성화된 것으로 판단되는데, 무기질비료 사용에 따른 토양의 산성화는 본 연구 외에도 다양한 연구에서 확인되고 있다(Lawson et al., 2013; Um et al., 2019). 토양 내 과도한 EC는 작물의 생장에 악영향을 주며, 적절한 조치를 취하지 못하면 생리적 장해로 인해 작물의 죽음을 초래한다(Lee et al., 2001). 또한 바이오차 처리 시 토양의 EC값을 상승시키는 것으로 보고되어 있다(Raison, 1979). 본 연구에 사용된 토양의 EC는 실험 후 모든 처리구에서 실험 전 토양(0.34 dS·m-1)에 비해 0.54 - 0.85 dS·m-1로 증가하였다. 이는 바이오차를 열분해하는 과정에 휘발성물질이 손실됨으로써 회분 내 다양한 염들이 농축되는 효과에 의해 EC가 증가되었을 것으로 판단된다(Cantrell et al., 2012). 탄소 함량의 경우 실험 전 토양의 0.49%에 비해 무처리구와 대조구에서는 감소하였으며, 바이오차 처리구에서는 증가하였다. 특히 pH 11.0 바이오차를 처리했을 때 약 1.40%로 가장 높은 탄소 격리 효과를 나타내었다. 토양 내 질소 함량은 실험 후 감소하였으며, 처리구간 유의차를 나타내지 않았다. 치환성 양이온(Mg2+, Ca2+, Na+, K+) 중 Mg2+는 실험 전 토양에 비해 실험 후 감소하였으며, Ca2+, Na+, K+는 실험 후 증가하였다.
바이오차의 화학적 특성 평가
바이오차의 pH가 NH3 배출에 미치는 영향을 평가하기 위해 제조 조건을 달리하여 바이오차의 pH를 구분하였다(Table 2). 바이오차의 pH는 열 분해 온도 및 시간이 증가함에 따라 증가하였으며, 350℃에서 15분 동안 열분해 시 pH 5.70으로 산성을 나타내었고, 600℃에서 30분간 열 분해 시 pH 11.0으로 강염기를 나타내었다. 바이오차의 T-C와 T-N은 pH와 유사하게 열 분해 조건이 증가함에 따라 증가하는 경향을 나타내었으며, T-H와 T-O는 pH와 대조적으로 감소하는 경향을 나타내었다. 바이오차의 H : C 비율과 O : C 비율은 각각 바이오차의 구조적 안정성과 극성 정도를 나타낸다(Oh and Chang, 2020). 본 연구에 사용된 바이오차의 H : C 비율은 1.16, 1.46, 0.41로 pH 11.0 바이오차는 H : C 비율이 0.7 이하이므로 토양에 처리시 구조적 안정성을 유지할 것으로 기대되며, pH 5.7 바이오차와 pH 6.7 바이오차는 반영구적으로 저장하기 어려울 것으로 판단된다(Kang et al., 2021). 바이오차의 O:C 비율은 바이오차의 pH가 증가함에 따라 0.69, 0.46, 0.12로 점차 감소하였으며, 이는 열 분해 과정에서 발생한 탈수 반응으로 바이오차의 친수성이 점차 감소함을 나타낸다(Oh and Chang, 2020). 바이오차의 T-P2O5는 pH 11.0 바이오차에서 가장 높았으며, pH 6.7 바이오차가 가장 낮은 함량을 나타내었다. 바이오차의 무기 조성(CaO, K2O, MgO, Na2O)는 pH가 증가함에 따라 대부분 증가하는 경향을 보였다.
Conclusion
본 연구는 pH가 다른 바이오차 처리가 농경지에서 발생하는 NH3에 미치는 영향을 평가하고자 하였다. 무기질비료를 처리한 토양에 바이오차(pH 5.7, 6.7, 11.0) 혼합 처리 시 농경지에서 발생하는 NH3 배출량을 저감시킬 수 있었다. 특히 pH 6.7 바이오차를 처리하였을 때 약 15, 25, 11%로 가장 높은 배출량 저감 효과를 나타내었으며, pH 5.7 바이오차를 처리 시 약 10, 19, 11%로 비교적 낮은 저감 효율을 나타내었다. 또한 요소 비료 기준량(320 kg·ha-1)을 시비하였을 때 바이오차의 NH3 저감 효율이 최대 약 25%로 가장 뛰어났다. 따라서 2차 미세먼지의 전구 물질인 NH3의 배출량 저감을 위해서는 pH 6.7 바이오차를 농경지 내 혼합 처리한 뒤, 요소를 기준량(320 kg·ha-1)처리하는 것이 NH3 배출량 저감에 가장 효과적일 것으로 사료된다.
Acknowledgements
본 논문은 농촌진흥청(Rural Development Administration of Korea)의 연구사업(세부과제번호: PJ01425302)의 지원에 의해 수행되었습니다.
Authors Information
Yun-Gu Kang, http://orcid.org/0000-0001-5368-5910
Jae-Han Lee, http://orcid.org/0000-0001-5761-2006
Jin-Hyuk Chun, http://orcid.org/0000-0002-3802-6834
Yeo-Uk Yun, Chungnam Agricultural Research and Extension Service, Agricultural researcher
Taek-Keun Oh, http://orcid.org/0000-0003-0215-0427
Jwa-Kyung Sung, http://orcid.org/0000-0002-0758-6644